

|
|
Главная -> Двухтактные карбюраторные двигатели 0 1 2 3 4 5 6 7 8 9 10 11 12 [13] 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 РАСЧЕТ ТОКСИЧНОСТИ ВЫПУСКНЫХ ГАЗОВ Характеристики токсичности двухтактных карбюраторных ДВС отличаются от аналогичных характеристик четырехтактных двигателей. У двухтактных двигателей большее значение имеют соединения свинца и углеводороды, меньшее - оксиды азота. По эмиссии монооксидов углерода двухтактные и четырехтактные ДВС находятся примерно в одинаковых условиях. Основным фактором, определяющим содержание СО в продуктах сгорания, является коэффициент а избытка воздуха. Характерное для двухтактных карбюраторных ДВС увеличение эмиссии СО на низких скоростных режимах связано с обогащением смеси. Однако при сгорании обедненных смесей в продуктах сгорания карбюраторных двигателей также содержится оксид углерода. Содержание оксида углерода в продуктах сгорания превышает стехиометрическое и при сгорании богатых смесей. Сверхстехио-метрическое содержание СО обусловлено наличием низкотемпературных пристеночных зон, в которых после начальных стадий окислительных реакций реакции окисления СО протекают слишком медленно, и диссоциацией молекул COg при высоких температурах сгорания. При понижении температуры происходит окисление СО в СОа по следующему неразветвленному цепному механизму: .. И ,6н f со; + 02< ,С0, "6 f со -СО, ОН f СО со, н о,(; fo,. 4Vi-co-co« (3.52) Наиболее медленная реакция, определяющая скорость окисления СО, СО + ОН СО2 I- Н. (3.53) Для горения оксида углерода необходимо присутствие радикалов ОН, которые могут образовываться, если в смеси есть водород или пары воды. При высокой температуре сгорания реакция протекает быстрее, чем изменяется температура, т. е. реакция находится в равновесном состоянии. С понижением температуры скорость реакции снижается и равновесное состояние не достигается. Температура стабилизации содержания СО зависит от состава смеси. С обогащением смеси она повышается, т. е. концентрация СО в продуктах сгорания увеличивается по сравнению со стехиометрической. Так как температура стабилизации содержания СО около 1000 К, то в двухтактных ДВС реакция, описываемая уравнением (3.53), отклоняется от равновесного состояния незначительно и при расчете можно поль.зоваться аналогично Р. Бен- сону поправочным коэффициентом. Расслоение СО в камерах его рания карбюраторных двигателей не превышает 10 % и его влиянием на образование СО можно пренебречь. Гак как в бензине азот практически отсутствует, существование в продуктах сгорания оксидов азота связано с окислением азота во.здуха. Согласно исследованию В. А. Звонова, из всех оксидов азота 99 % в карбюраторных двигателях составляет монооксид N0. Образование NO2 происходит в основном в выпускных тру бах и в атмосфере. Поэтому при исследовании образования токсичных продуктов сгорания азота можно учитывать только N0. Образование N0 из азота воздуха имеет термическую природу и по сведениям Я. Б. Зельдовича происходит в основном по нераз-ветЕленной цепной реакции N0 N0 ... O-f N2 --N f 02~>-0 [\ + О -- N0 + N 316 МДж/кмоль; N f (\ по 4 О Н 136 МДж/кмоль; (3.54) (3.55) (3.56) (3.57) в суммарном виде N. i О, Tfc 2N0 - 180 МДж/кмоль. Добавив к уравнениям (3.55) и (3.56) уравнение реакции, учитывающее влияние монорадикала ОН, получим расширенный механизм Я. Б. Зельдовича: N I- ОМ =F* N0 I- И f 207 МДж/кмоль. (3.58) Приведенное ,1.ж. Хейвудом сравнение скоростей реакций по уравнениям (3.55), (3.56) и (3.58) при обедненной, стехиометрической и обогащенной смеси подтверждает большое значение реакции, описываемой уравнением (3.58), особенно при обогащенной смеси. В большей или меньшей степени в продуктах сгорания присутствуют следующие компоненты: СО, СО3, N2, N0, NgO, N, Hj, И, HgO, ОН, О2, NHg, HNO3, О, разные углеводороды. При рассмотрении образования СО и N0 по В. Эннэнду наиболее важными т них являются следующие одинчадп,ять: СО, COj, Nj, N. NO, Н„ Н, ОН, О2, О, Н2О. Концентрации радикалов кислорода, водороа и ОН опреде-.лтуусм в ofп<PI!lV реакпиями: 1L 1 О ОН Н„ М Н Ч- Н 4 М; (3.59) (3.60) Н, 1 ОН Н,Р i Н. (3.61) Окисление СО происходит согласно реакции (3.53). Все компоненты, кроме мопооксида азота, во время сгорания ч расширения на.одягм пргичгическн в рарловесном состоянии. Это позволяет вывести уравнения для определения их концентрации на основании закона действующих масс. Из стехиометриче-ских уравнений (3.53), (3.55), (3.56), (3.58)-(3-61) получаем семь уравнений для определения молярной концентрации С отдельных компонентов:
где К\ ... Кт-- коэффициенты равновесия. В отличие от других коэффициентов равновесия Кь измеряется в кмоль/м. Для расчета содержания одиннадцати компонентов в смеси к приведенным семи уравнениям необходимо добавить четыре уравнения баланса: кислорода (весь кислород свежей смеси расходуется на образование СО2, СО, Оа, НО, ОН и N0) Ссо.+ СО -н,о 12 i/ i/ (3.69) водорода (весь водород топлива расходуется на образование Н, Н, ОН и НаО) г 1 И , ОН ЬИ. -г -о- Т--9~ азота углерода + "•0 -т-т;sI;p7/ 2i - о 70 !ДгКл.- о i/ i/ > Ссо-Ссо.=-~--~!, (3.70) (3.71) (3.72) где x - доля выгоревшего топлива; Vp - объем продуктов сгорания; - объем одного киломоля газа при нормальных условиях; Я - массовая доля водорода в топливе; Lq - стехиометричб-ское соотношение; С - массовая доля углерода в топливе. Реакции образования монооксида азота обратимые, при росте температуры концентрация N0 увеличивается. Скорость образования N0 зависит от концентрации атомарного кислорода, т. е. и от содержания О. Максимальное содержание N0 в продуктах 86 сгорания поэтому соответствует некоторой обедненной смеси (а = 1,05 ... 1,1). При обогащении смеси, хотя температура (до а W 0,95) повышается ввиду недостатка кислорода, содержание N0 в продуктах сгорания уменьшается, Энергия активации образования N0 по уравнению (3.55) превышает 500 МДж/кмоль: скорость реакции очень сильно зависит от температуры. Снижение температуры от 2600 до 1500 К приводит при прочих равных условиях к уменьшению скорости реакции в 3,7-10° раза. Вследствие такой сильной зависимости реакции образования N0 от температуры при быстром охлаждении продуктов сгорания в такте расширения происходит стабилизация содержания в них N0. На эмиссию N0 влияют цикловые колебания и Махе-эффект. Однако ввиду пониженной (по сравнению с четырехтактными двигателями) эмиссии N0 этими явлениями можно пренебречь. Сильная зависимость скорости окисления азота от температуры обусловливает необходимость учета отклонения этих реакций от равновесного состояния. Исследования показали, что неравновесная концентрация N0 в двигателях с искровым зажиганием определяется также достаточно точно расширенным механизмом Я. Б. Зельдовича. Доля бимолекулярной реакции (3.57) по В. А. Звонову относительно незначительная. Изменение молярной концентрации оксида азота Cfo вызвано реакциями N0 и изменением объема продуктов сгорания Vp (С используем для обозначения неустановившейся молярности): (3.73) Предполагая, что концентрация всех компонентов, кроме N0 и N, соответствует равновесной, а атомарное содержание азота в первом приближении стационарное, получаем
dHO 2(l--a) „ dVp - =-«1---г-- x0-f 1 (3.74) где X = -n r-D S = ktCfio = iCnCno - установившаяся Ki + скорость реакции по уравнению (3.55); R2 = ICnCo, = = к/СыоСо - установившаяся скорость реакции по уравнению (3.56); Яъ = ktCCoH = кзСпоСц - установившаяся скорость реакции (3.58); а = Cno /Cno; о = Cn/Cn. Уровень концентрации углеводородов СН в выпускных газах двухтактных ДВС значительно выше, чем в четырехтактных. На полной нагрузке объемная доля СН доходит до 4000 ... 8000 млн". Основной причиной наличия углеводородов в выпускных газах принято считать гашение пламени в относительно холодных пристеночных слоях смеси. Гашение пламени подтверждается анализом газа, взятого из пристеночного слоя, а также оптиче- 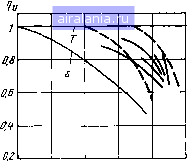 СН,млн- 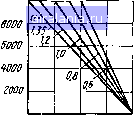 0,Z 0Л 0,6 0,8 Рис. 3.16. Показатели продувки двигателя (s - полное смешивание; Т - послойное вытеснение): --экспериментальные данные;------ расчетные данные О.г ОЛ 0,6 0.8 /1ц Рис. 3.17. Влияние качества продувки на эмиссию углеводородов скими измерениями. Это явление возможно в зазоре поршень - цилиндр, над поршневым кольцом. Из пристеночного слоя и из зазора поршень - цилиндр углеводороды вместе с продуктами сгорания вытекают из цилиндра, реагируют со свободным кислородом, а частично остаются в цилиндре. Кроме того, в двухтактных двигателях выход углеводородов с выпускными газами в атмосферу обуппвлен следующим: потери свежей смеси во время продувки (ti < 1, рис. 3.16) являются основной причиной низкой экономичности и высокой эмиссии углеводородов двухтактных ДВС. Как подтверждают результаты расчетов (рис. 3.17), даже на относительно экономичном рабочем режиме (т]и = 0,8, а = 1,1) объемная доля углеводородов в выпускных газах от потерь свежей смеси составляет около 2600 млн". При увеличении потерь (ти = 0,7, а = 0,7) выброс СН возрастает до 7000 млн". Полученные результаты хорошо коррелируются с экспериментальными данными; пропусками вспышек, особенно на низких нагрузках и скоростях ввиду высокого коэффициента остаточных газов. По исследованиям Г. Ямагиси при дросселировании двухтактных ДВС пропуски зажигания начинаются примерно при фо = 0,3, а при Фо < 0,2 пропускается уже 50% циклов. Как показали исследования С. Кинсуке, добавка масла к топливу не является причиной высокой эмиссии углеводородов в двухтактных ДВС. При увеличении объемной доли масла в смеси от 0,5 до 3 % (1:200...1:33) изменений в эмиссии углеводородов практически не наблюдается. Однако смазывание смесью обусловливает около 90 % дымности ДВС. Вследствие потерь свежей смеси (тв == 0,7...0,8) температура раза в выпускной системе двухтактного двигателя относительно 88 низкая. Поэтому у двигателей без термических реакторов в выпускной системе концентрация углеводородов в ОГ существенно не понижается. Можно считать, что содержание углеводородов в выпускных газах в основном определяется процессами в цилиндре. На полной нагрузке количество СН в ОГ, обусловленное неполнотой сгорания топлива в цилиндре, определяется объемом jOH гашения пламени. С учетом того, что углеводороды из зон гашения пламени составляют у двухтактных ДВС относительно малую долю, можно расчет их количества вести приближенно. Согласно данным Дж. Хейвуда толщину пристеночного слоя гашения пламени можно выразить эмпирической формулой б.40.07-.-0,08) (3.75) Объемную долю углеводородов в пристеночном слое можно рассчитать как для свежей смеси (на полной нагрузке коэффициент 7г остаточных газов относительно низкий): си о = а/.оЦт (3.76) где Рт - молярная масса топлива. Объемная доля углеводородов в продуктах сгорания, вытекающих из цилиндра, определяется по массовому содержанию углеводородов в цилиндре и коэффициенту С„р продувки пристеночного слоя; сн о Рр. 8314Г„ (3.77) где Рц - давление в цилиндре; f„ - площадь поверхностей камеры сгорания; Af, - количество смеси, кмоль/кг; - коэффициент молекулярного изменения свежей смеси. Объемная доля t-ro компонента в выпускных газах г, - (3.78) где ла - объемная доля компонента в свежей смеси; Л(ц - объемная доля компонента в продуктах сгорания. Для СН объемную долю Гц определяют из (3.77), для N0 - с помощью (3.74), а для остальных компонентов - из условий равновесия. С вводом в уравнения, определяющие токсичность ОГ двигателя, безразмерных переменных и обозначением неравновесного содержания N0 через N0 получается система уравнений в обоб-uieHHOM виде: 0 1 2 3 4 5 6 7 8 9 10 11 12 [13] 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 0.0066 |